Fonte: REVISTA FAPESP
Texto: Ricardo Zorzetto | Pesquisa FAPESP
Nazareno Scaccia calçou um par de luvas, apanhou um balde de aço esterilizado e o atou à extremidade de uma corda. Em seguida, baixou-o até o fundo da galeria que recebe o esgoto dos bairros centrais de São Caetano, na Região Metropolitana de São Paulo, antes de içá-lo cheio de uma água levemente turva, com coloração amarela-acastanhada e odor desagradável. Armazenou o líquido em um galão plástico e usou uma seringa acoplada a um filtro para preencher um pequeno frasco. “Fazemos isso para separar os microrganismos e evitar que degradem os compostos químicos presentes na água”, explicou o microbiologista italiano, que faz estágio de pós-doutorado na Faculdade de Medicina da Universidade de São Paulo (FM-USP). Algumas bactérias são capazes de digerir o princípio ativo dos antibióticos, o que atrapalha a detecção desses compostos na água.
Naquela manhã de 6 de novembro, Scaccia e as biólogas Miriam Lopes da Silva e Francisca Peternella ainda percorreriam outros oito pontos da cidade vizinha a São Paulo repetindo o procedimento. A água coletada da torneira, de riachos e do esgoto comum e hospitalar seria depois levada a um laboratório na Faculdade de Saúde Pública (FSP) da USP para verificar a presença de bactérias resistentes a antibióticos. O trabalho é parte de um projeto internacional, coordenado no Brasil pela infectologista Anna Sara Levin, da FM-USP, que se destina a avaliar se a prescrição e o uso adequado desses medicamentos podem reduzir o surgimento e a dispersão de microrganismos contra os quais os antibióticos não produzem mais o efeito desejado.
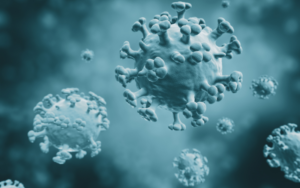
A disseminação de bactérias e outros microrganismos resistentes a quase todos os antimicrobianos disponíveis é um pesadelo mundial. Ela ocorre desde que os primeiros antibióticos começaram a ser usados e avança rapidamente, tirando o sono dos especialistas por representar uma ameaça a uma das maiores conquistas da medicina moderna: a capacidade de debelar infecções. Sem antibióticos eficientes, fica quase impossível realizar cirurgias, transplantes e tratamentos quimioterápicos contra o câncer em segurança. Problemas comuns, como um corte mais profundo ou uma infecção respiratória, podem se tornar uma ameaça à vida.
“Poucas intervenções aumentaram tanto a longevidade humana quanto a oferta de água tratada e o desenvolvimento de vacinas e antibióticos”, conta o infectologista Arnaldo Lopes Colombo, da Universidade Federal de São Paulo (Unifesp), que coordena o Instituto Paulista de Resistência aos Antimicrobianos, um dos Centros de Pesquisa, Inovação e Difusão (Cepid) apoiados pela FAPESP. Algumas estimativas indicam que o uso de antibacterianos para tratar infecções aumentou a longevidade humana em cerca de 20 anos.
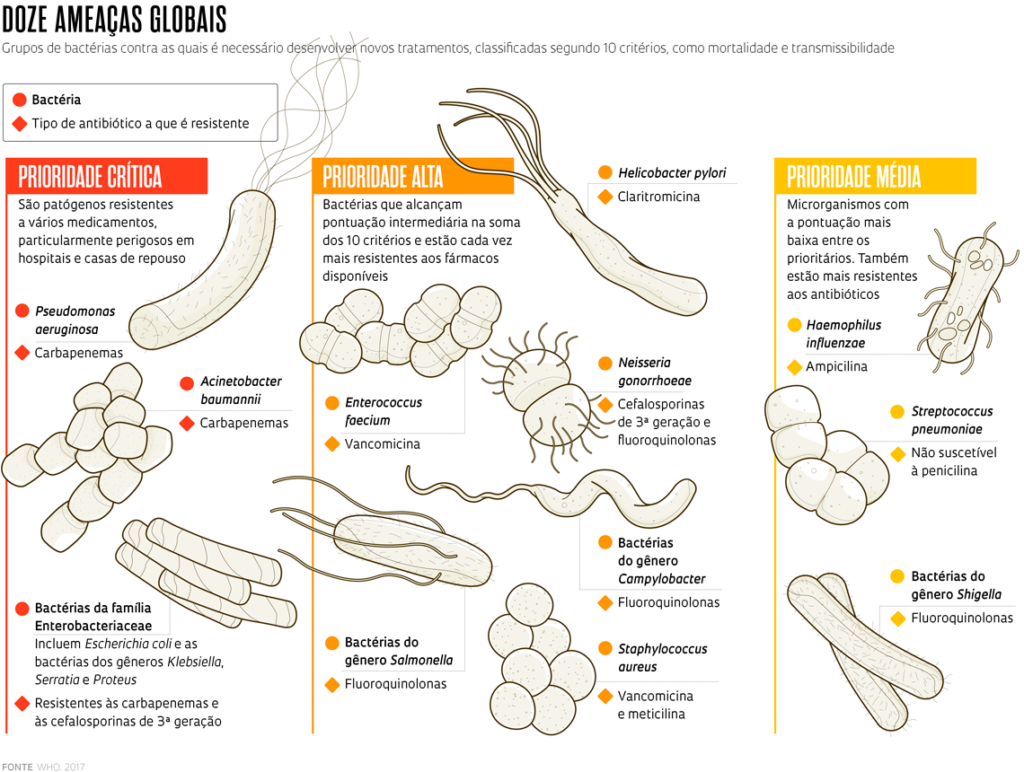
Antibióticos são compostos químicos que inibem o crescimento de bactérias ou as matam. Agem apenas contra esses microrganismos, e não funcionam, por exemplo, contra vírus. Tecnicamente, o termo é usado para definir os compostos de origem natural (produzidos por fungos ou outras bactérias) que eliminam bactérias patogênicas. Popularmente, no entanto, ele é empregado para as moléculas sintéticas ou semissintéticas que exterminam esses microrganismos. Há cerca de 12 classes de antibióticos. Cada uma atua em um ponto diferente da estrutura ou do funcionamento das bactérias (ver infográfico).
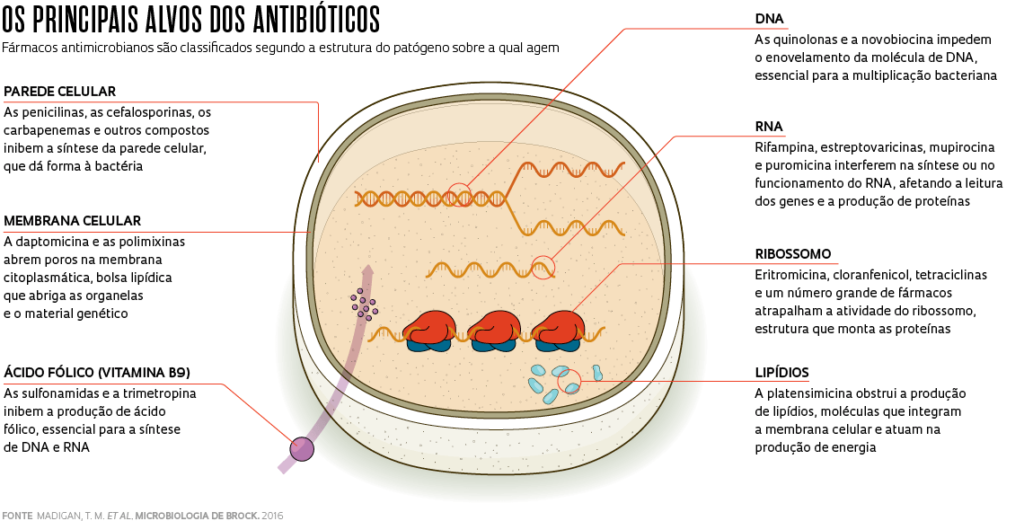
Expostas à concentração adequada dos antibióticos e por tempo suficiente, as bactérias facilmente morrem. Se a dosagem e duração do tratamento forem inferiores ao necessário para aniquilá-las, uma parte pode sobreviver e se multiplicar, acumulando alterações no material genético que permitem escapar à ação dos fármacos.
As bactérias estão em todos os lugares: na água, no solo, no ar e nas superfícies, inclusive do nosso corpo. Com o uso intensivo de antibióticos na saúde humana e na produção de alimentos, para proteger ou tratar os animais de criação de doenças e induzir ganho de peso, as bactérias são continuamente expostas a esses fármacos. Esse contato favorece a seleção das variedades resistentes.
“Estamos vendo surgir bactérias contra as quais não há mais medicamentos eficazes”, relata a infectologista brasileira Fernanda Lessa, chefe do programa internacional de controle de infecções dos Centros de Controle e Prevenção de Doenças (CDC) dos Estados Unidos. Ela coordenou um suplemento especial sobre o assunto, publicado em julho de 2023 na revista Clinical Infectious Diseases, e afirma: “Por sorte as infecções causadas por esses microrganismos ainda são relativamente raras na comunidade e estão quase sempre restritas aos hospitais”.
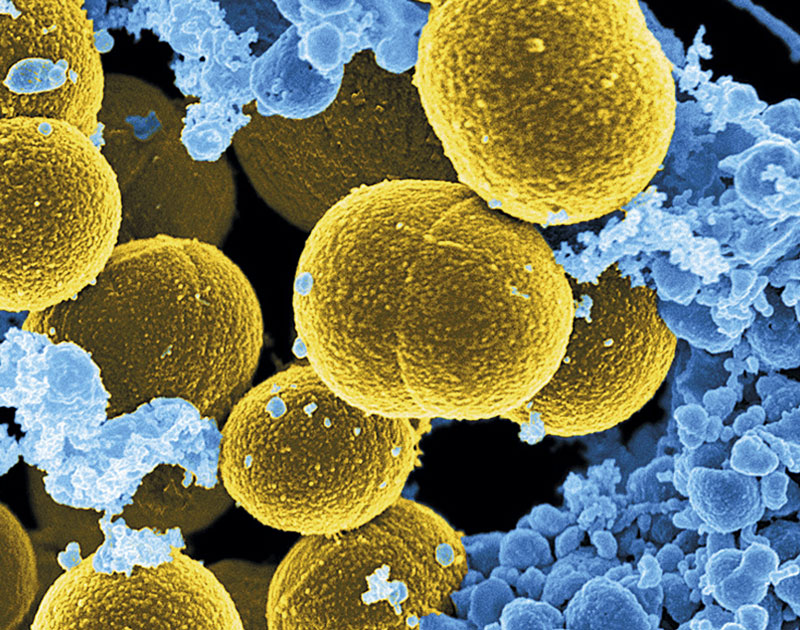
Frank De Leo / NIAID
Mesmo assim, as infecções por bactérias resistentes a múltiplos medicamentos – também chamadas de multirresistentes ou superbactérias – causam um estrago enorme. Um levantamento coordenado pelo epidemiologista Ramanan Laxminarayan, da Universidade de Princeton, nos Estados Unidos, estimou que, a cada ano, no mundo, ocorram 136 milhões de casos de infecção hospitalar causados por esses microrganismos. Segundo os dados, publicados em junho de 2023 na revista PLOS Medicine, a China é, de longe, a nação mais afetada, com 52 milhões de registros. O Brasil aparece em quinto lugar, com 4 milhões de casos.
No mundo todo, esses microrganismos foram os responsáveis diretos por 1,27 milhão de mortes em 2019. Quando se incluem os casos em que o indivíduo tinha outra doença além da infecção, esse número sobe para 4,95 milhões, próximo ao total de óbitos registrados em três anos de pandemia de Covid-19 e bem superior à soma das mortes anuais por malária, Aids e tuberculose.
Essas cifras foram calculadas por um grupo internacional de pesquisadores, do qual participaram brasileiros, com base em dados de 204 países. Publicado em 2022 na revista The Lancet, o trabalho mostra que quase 80% dos óbitos decorreram de infecções no trato respiratório inferior (bronquites e pneumonias), no sistema circulatório ou na cavidade abdominal.
Seis espécies de superbactérias foram responsáveis por ao menos 70% das mortes: Escherichia coli, Staphylococcus aureus, Klebsiella pneumoniae, Streptococcus pneumoniae, Acinetobacter baumannii e Pseudomonas aeruginosa. Todas integram a lista de patógenos prioritários, publicada em 2017 pela Organização Mundial da Saúde (OMS), contra os quais é preciso desenvolver novos antibióticos.
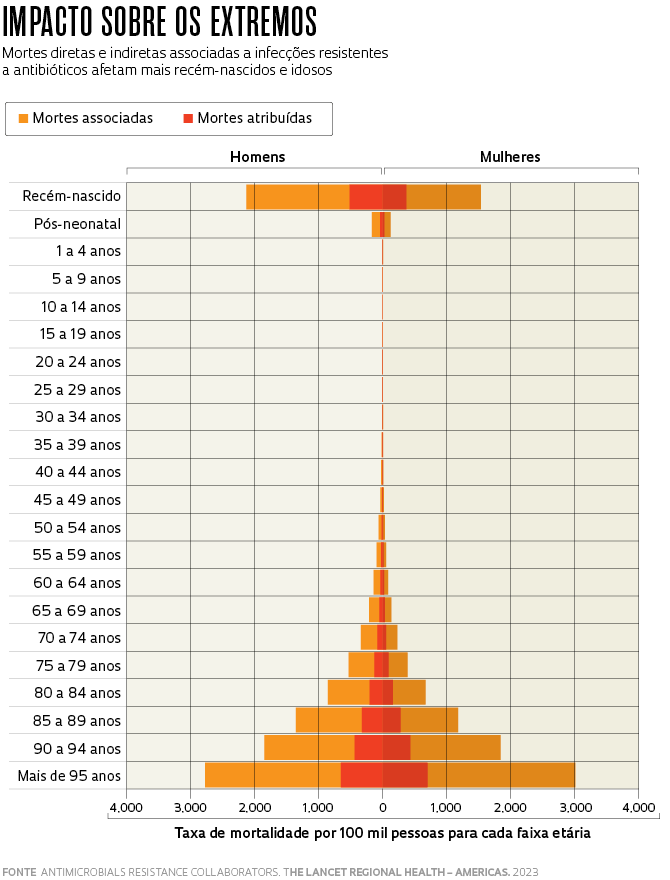
Com 14% da população mundial, os 35 países das Américas concentram aproximadamente 11% das mortes por infecções bacterianas resistentes a antibióticos. Foram 141 mil óbitos diretamente provocados por esses microrganismos e 569 mil associados a eles em 2019, segundo estudo publicado em agosto de 2023 na revista The Lancet Regional Health – Americas. Novamente, a grande maioria (80%) foi causada pelos seis patógenos. As ocorrências, em números absolutos, estão concentradas nas nações mais populosas: Estados Unidos e Brasil. Aqui, foram 33,2 mil mortes (cerca de 90 por dia) diretamente causadas por infecções resistentes e 138 mil nas quais as superbactérias tiveram alguma participação. “Os grupos mais afetados estão nos extremos da pirâmide etária da nossa população, os bebês de até 1 mês de vida e as pessoas com mais de 65 anos”, conta o pediatra Eitan Berezin, da Faculdade de Medicina da Santa Casa de São Paulo, um dos autores do estudo.
“Suspeito que hoje o número de mortes no Brasil e no mundo seja ainda mais elevado”, relatou Lessa, do CDC, em entrevista por videochamada em setembro. “Esses estudos usaram dados de 2019 e na pandemia de Covid-19 aumentou o consumo de antibióticos”, disse.
Dois estudos coordenados por ela e publicados em julho na Clinical Infectious Diseases indicaram essa tendência. Em um dos trabalhos, Lessa e colaboradores analisaram os registros de dispensação desses medicamentos em seis hospitais – dois no Brasil, dois no Chile e dois na Argentina – em dois períodos: entre março de 2018 e fevereiro de 2020 e no primeiro ano da pandemia. Com o aumento das internações após o surgimento do novo coronavírus, o uso de antibióticos cresceu nos seis hospitais (até 35%), algo antes observado nos Estados Unidos. No Brasil, também aumentaram as prescrições de antibióticos para tratar infecções respiratórias na comunidade. Entre janeiro de 2019 e março de 2020, foram receitados 19,9 milhões de doses, no primeiro ano da pandemia, 27,5 milhões, de acordo com o segundo estudo.
Antes mesmo do aparecimento do novo coronavírus já havia sinais do crescimento do consumo desses medicamentos no mundo. Laxminarayan, de Princeton, e colaboradores rastrearam a venda de antibióticos em 76 países de 2000 a 2015 e observaram dois efeitos. O primeiro foi um aumento de 65% na quantidade consumida, de 21,1 bilhões para 34,8 bilhões de doses diárias, segundo estudo publicado em 2018 na revista PNAS. O segundo é que cresceu quase 40% a proporção de pessoas usando esse tipo de medicamento: havia 11,3 doses diárias para cada mil habitantes em 2000 e 15,7 por mil em 2015. A elevação foi puxada pela melhora econômica em países de média e baixa renda. Apesar da subida, estima-se que 6 milhões de pessoas morram por ano no mundo por falta de acesso a antibióticos.
O aumento no uso desses fármacos, intensificado na pandemia, e a superlotação dos hospitais parecem ter contribuído para a dispersão de genes que permitem às bactérias se livrar de medicamentos.
No Brasil, essa tendência foi observada pelo infectologista Carlos Kiffer, da Unifesp, e colaboradores da Pontifícia Universidade Católica do Paraná (PUC-PR) e da Fundação Oswaldo Cruz (Fiocruz). Eles analisaram os dados provenientes de testes genéticos de mais de 80 mil amostras de bactérias coletadas em hospitais de quase todo o país de 2017 a 2022 e constataram que, na pandemia, houve um aumento significativo (de 4 a 21 pontos percentuais) na frequência de genes que conferem a oito espécies de bactérias resistência aos carbapenêmicos, antibióticos considerados o último recurso para tratar infecções hospitalares graves. Klebsiella pneumoniae, Escherichia coli e Acinetobacter baumannii estavam entre os principais microrganismos, segundo o trabalho, publicado em julho na Clinical Infectious Diseases. “Havia evidências pontuais de que alguns desses genes estavam se tornando mais comuns no país. Ajudamos a dimensionar o problema”, conta Kiffer.
Para a infectologista Anna Levin, da USP, coordenadora do projeto de rastreamento citado no início desta reportagem, a ocorrência de infecções hospitalares por bactérias resistentes é um reflexo da qualidade do atendimento. “Quando o sistema está no limite, com excesso de pacientes e poucos profissionais para atender, as taxas de infecção aumentam”, afirma a pesquisadora, que preside a comissão de controle de infecção do Hospital das Clínicas da USP, o maior complexo de saúde do país. Durante a pandemia, o grupo de Levin conseguiu controlar a disseminação de infecções por bactérias multirresistentes no pronto-socorro do hospital ao submeter as pessoas que eram internadas a testes de detecção dos patógenos e isolar aquelas colonizadas, tratando-as separadamente.
Embora a resistência a antibióticos seja um problema antigo, só recentemente o mundo passou a prestar atenção a ele, por causa de dois documentos: um relatório de 2014 da OMS, que mostrou que o fenômeno estava disseminado pelo planeta, e um estudo conduzido pelo economista James O’Neill, a pedido do governo do Reino Unido, que projetou um cenário catastrófico para 2050. Se nada for feito, as infecções resistentes aos antibióticos deverão causar 10 milhões de mortes por ano na metade do século e provocar perdas na economia que podem chegar a US$ 100 trilhões.
Em sua edição de 2016, o livro Microbiologia de Brock, adotado em cursos da área da saúde, informa que ao menos 10 mil toneladas de antibióticos são produzidas por ano no mundo e utilizadas na saúde humana e animal. Uma consequência é que esses produtos, mesmo quando usados de forma correta, contaminam o ambiente, favorecendo o surgimento de bactérias resistentes. “No Brasil, não é obrigatório tratar o esgoto hospitalar para a eliminação de bactérias presentes na urina e fezes dos pacientes ou no ambiente hospitalar. Não temos um bom sistema de vigilância que integre a frequência de microrganismos resistentes nos hospitais e monitore a sua disseminação para a comunidade e o meio ambiente”, conta Ana Gales, a infectologista da Unifesp que estuda o assunto.

Léo Ramos Chaves / Revista Pesquisa FAPESP
Nos últimos anos, uma série de trabalhos trouxe evidências de que o problema que deveria ser predominantemente hospitalar já se acentuou no ambiente. A equipe da farmacêutica bioquímica Eliana Stehling, da Faculdade de Ciências Farmacêuticas de Ribeirão Preto da USP, acompanha a dispersão de bactérias multirresistentes a antibióticos em quase 50 cidades no norte do estado e já detectou esses microrganismos em amostras de solos de áreas agrícolas e de criação de animais, além de águas de rios, córregos e riachos. “No ambiente, em especial na água, esses fármacos podem selecionar superbactérias, acelerando a dispersão da resistência antimicrobiana, uma vez que esses microrganismos trocam material genético entre si”, conta o farmacêutico João Pedro Furlan, do grupo de Ribeirão Preto.
No campus de São Paulo da USP, o microbiologista chileno Nilton Lincopan e sua equipe já identificaram bactérias resistentes onde quer que se possa imaginar. Elas estão na água dos rios Tietê e Pinheiros, que cortam a capital, e infectando tartarugas, pinguins, baleias e golfinhos, além de aves marinhas, no litoral brasileiro. “Registramos uns 30 casos nos últimos quatro anos”, conta o pesquisador.
Também foram encontradas em cães e gatos atendidos em clínicas e hospitais veterinários da cidade e em amostras de alface, rúcula e repolho frescos vendidos no principal entreposto comercial de São Paulo. “Algumas variedades são resistentes ao ambiente ácido. Isso significa que podem sobreviver à passagem pelo estômago e colonizar o intestino de quem come uma verdura mal lavada”, explica Lincopan.
O fenômeno que se observa há mais tempo entre as bactérias ocorre também com os fungos, embora seja mais difícil de mensurar pela falta de dados. Por essa razão, em 2022, a OMS lançou a primeira lista de patógenos fúngicos prioritários para planejamento de ações de saúde pública. Nela, foi incluída a levedura Candida auris, que vem causando surtos em hospitais de todos os continentes. “As infecções por fungos multirresistentes aos medicamentos existentes são menos comuns, mas podem ser mais letais que as bacterianas”, afirma Colombo, da Unifesp, um estudioso do problema.
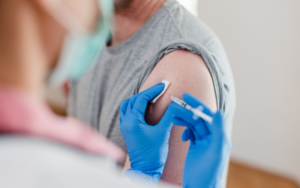
Diante desse cenário, os especialistas recomendam algumas medidas. As mais simples e abrangentes, a serem praticadas por todos, são realizar boa higiene pessoal e dos alimentos, além de se vacinar contra os microrganismos para os quais há imunizante, como certas bactérias causadoras de pneumonia, tuberculose e meningite. Outra é usar de modo otimizado e rigoroso os medicamentos. Os médicos devem prescrever antibióticos apenas para as infecções bacterianas, se possível com o auxílio de testes que permitam saber qual o fármaco mais adequado para cada caso, e antifúngicos para as infecções por fungos. Já o paciente deve usar a dose recomendada e pelo tempo indicado, mesmo que melhore antes. Sempre que possível, o ideal é manter-se longe dos hospitais e, quando necessário, passar neles o menor tempo possível.
Projetos
1. Instituto Paulista de Resistência aos Antimicrobianos (Projeto Aries) (nº 21/10599-3); Modalidade Centros de Pesquisa, Inovação e Difusão (Cepid); Pesquisador responsável Arnaldo Lopes Colombo (Unifesp); Investimento R$ 15.021.964,28.
2. Rede multidisciplinar internacional para caracterização de aspectos microbiológicos e da história natural de Infecções Fúngicas Invasivas (IFI) por espécies do gênero Candida (nº 17/02203-7); Modalidade Projeto Temático; Pesquisador responsável Arnaldo Lopes Colombo (Unifesp); Investimento R$ 1.328.821,49.
3. Rastreamento e isolamento precoce de pacientes colonizados por enterobactérias resistentes a carbapenêmicos admitidos no pronto-socorro (nº 18/06016-0); Modalidade Auxílio à Pesquisa – Regular; Pesquisador responsável Icaro Boszoczowski (FM-USP); Investimento R$ 114.610,59.
4. Resistoma, plasmidoma e viruloma de Enterobacterales isoladas do meio ambiente carreando genes mcr-like (nº 21/01655-7); Modalidade Auxílio à Pesquisa – Regular; Pesquisadora responsável Eliana Guedes Stehling (USP-RP); Investimento R$ 199.956,01.
5. Estudo do perfil de resistência, virulência e epidemiológico de Escherichia coli isoladas do meio ambiente (nº 18/01890-3); Modalidade Bolsa de Doutorado; Pesquisadora responsável Eliana Guedes Stehling (USP-RP); Bolsista João Pedro Rueda Furlan; Investimento R$ 150.141,19.
6. One Health Brazilian Resistance (OneBR): Base genômica integrada para vigilância, diagnóstico e tratamento da resistência aos antimicrobianos na interface humana-ambiente-animal, no Brasil (nº 20/08224-9); Modalidade Auxílio à Pesquisa – Regular; Pesquisador responsável Nilton Erbet Lincopan Huenuman (USP); Investimento R$ 241.806,62.
7. Viruloma e patogenicidade de linhagens bacterianas prioritárias em saúde única resistentes a carbapenêmicos e polimixinas (nº 19/15578-4); Modalidade Bolsa de Doutorado; Pesquisador responsável Nilton Erbet Lincopan Huenuman (USP); Bolsista Fernanda Ribeiro dos Santos Esposito; Investimento R$ 190.601,93.
8. Pan-resistoma de Klebsiella pneumoniae e Escherichia coli produtoras de beta-lactamases (KPC-2, CTX-M-8, CTX-M-15) endêmicas no Brasil (nº 16/08593-9); Modalidade Auxílio à Pesquisa – Regular; Pesquisador responsável Nilton Erbet Lincopan Huenuman (USP); Investimento R$ 214.075,41.
9. Análise comparativa do resistoma de Klebsiella pneumoniae XDR (NDM-1/KPC-2) pertencente ao complexo clonal (CC) endêmico de alto risco CC258 (nº 15/21325-0); Modalidade Bolsa de Doutorado; Pesquisador responsável Nilton Erbet Lincopan Huenuman (USP); Bolsista Louise Teixeira Cerdeira; Investimento R$ 131.634,25.
Artigos científicos
BALASUBRAMANIAN, R. et al. Global incidence in hospital-associated infections resistant to antibiotics: An analysis of point prevalence surveys from 99 countries. PLOS Medicine. 13 jun. 2023.
ANTIMICROBIAL RESISTANTE COLLABORATORS. Global burden of bacterial antimicrobial resistance in 2019: A systematic analysis. The Lancet. 19 jan. 2022.
WHO. Prioritization of pathogens to guide discovery, research and development of new antibiotics for drug-resistant bacterial infections, including tuberculosis. 4 set. 2017.
ANTIMICROBIAL RESISTANTE COLLABORATORS. The burden of antimicrobial resistance in the Americas in 2019: A cross-country systematic analysis. The Lancet Regional Health ‒ Americas. 8 ago. 2023.
PATEL, T. S. et al. Trends in inpatient antibiotic use among adults hospitalized during the coronavirus disease 2019 pandemic in Argentina, Brazil, and Chile, 2018-2021. Clinical Infectious Diseases. 5 jul. 2023.
SOLANKY, D. et al. Prescribing of outpatient antibiotics commonly used for respiratory infections among adults before and during the coronavirus disease 2019 pandemic in Brazil. Clinical Infectious Diseases. 5 jul. 2023.
KLEIN, E. Y. et al. Global increase and geographic convergence in antibiotic consumption between 2000 and 2015. PNAS. 26 mar. 2018.
KIFFER, C. R. V. et al. A 7-Year Brazilian national perspective on plasmid-mediated carbapenem resistance in Enterobacterales, Pseudomonas aeruginosa, and Acinetobacter baumannii complex and the impact of the coronavirus disease 2019 pandemic on their occurrence. Clinical Infectious Diseases. 5 jul. 2023.
FURLAN, J. P. R. et al. Genetic plurality of blaKPC-2-harboring plasmids in high-risk clones of Klebsiella pneumoniae of environmental origin. Science of the Total Environment. 10 jul. 2023.
FURLAN, J. P. R. et al. Early dissemination of novel NDM-1-producing Klebsiella pneumoniae ST6326 to the environment. Journal of Global Antimicrobial Resistance. set. 2023.
FURLAN, J. P. R. et al. Detection of CTX-M-27-positive endophytic Escherichia coli ST131 lineage C1/H30R subclade carrying blaKPC-2 on an IncX3-IncU plasmid in a fresh vegetable. Journal of Global Antimicrobial Resistance. 20 jun. 2022.
FURLAN, J. P. R. e STEHLING, E. G. Multiple sequence types, virulence determinants and antimicrobial resistance genes in multidrug- and colistin-resistant Escherichia coli from agricultural and non-agricultural soils. Environmental Pollution. 1º nov. 2021.
ESPOSITO, F. et al. Genomic analysis of carbapenem-resistant Pseudomonas aeruginosa isolated from urban rivers confirms spread of clone sequence type 277 carrying broad resistome and virulome beyond the hospital. Frontiers in Microbriology. 3 set. 2021.
LOPES, F. et al. Endophytic lifestyle of global clones of extended-spectrum β-lactamase-producing priority pathogens in fresh vegetables: A trojan horse strategy favoring human colonization? mSystems. 9 fev. 2021.
DA SILVA, L. C. B. A. et al. Human pandemic K27-ST392 CTX-M-15 extended-spectrum β-lactamase-positive Klebsiella pneumoniae: A one health clone threatening companion animals. One Health. 3 jul. 2022.
EWBANK, A. C. et al. World Health Organization critical priority Escherichia coli clone ST648 in magnificent frigatebird (Fregata magnificens) of an uninhabited insular environment. Frontiers in Microbiology. 11 ago. 2022.
SANO, E. et al. One health clones of multidrug-resistant Escherichia coli carried by synanthropic animals in Brazil. One Health. 21 dez. 2022.
MARTINS, W. M. B. S. et al. SPM-1-producing Pseudomonas aeruginosa ST277 clone recovered from microbiota of migratory birds. Diagnostic Microbiology and Infectious Disease. mar. 2018.
NARCISO, A. C. et al. Healthcare-associated carbapenem-resistant OXA-72-producing Acinetobacter baumannii of the clonal complex CC79 colonizing migratory and captive aquatic birds in a Brazilian zoo. Science of the Total Environment. 15 jul. 2020.
NARCISO, A. C. et al. Detection of OXA-58-producing Acinetobacter seifertii recovered from a black-necked swan at a zoo lake. Antimicrobial Agents and Chemotherapy. 22 nov. 2017.
PICÃO, R. C. et al. The route of antimicrobial resistance from the hospital effluent to the environment: Focus on the occurrence of KPC-producing Aeromonas spp. and Enterobacteriaceae in sewage. Diagnostic Microbiology and Infectious Disease. mai. 2013.
WHO. WHO fungal priority pathogens list to guide research, development and public health action. 25 out. 2022.